硬件包括哪些设备英文单词硬件防火墙原理
COCIR调查了欧盟国家CT、MR、X射线血管造影/介入机和PET等各类影像设备的使用状况……

COCIR调查了欧盟国家CT、MR、X射线血管造影/介入机和PET等各类影像设备的使用状况。
调查结果发现,大约有20%的设备服役超过10年。这类设备很难得到正确的维护和修复,更令人担忧的是,许多现代程序在这类设备上运行时也不尽如人意。
这些老化的设备包括大约2900台CT、2100台磁共振、1800台X射线台PET,它们的使用年限均已达到或超过10年。
COCIR希望各国政府和欧盟政策制定者能够支持更换老化设备。在过去的十年时间里,符合COCIR“金标准”的国家数量并没有显著增加,事实上,CT和磁共振设备的老化情况还在进一步恶化。
没有一种医疗设备可以永远使用。在其生命周期的某个阶段,某款设备总会被替换,为更新、更先进的型号让路。但是在被拆卸(de-installed)之后,这些设备也并不一定需要报废,它们可能还有利用价值——翻新再造。
欧美国家强调的是完全再造,即完全按照COCIR的医疗设备GRP再造规范进行翻新,确保翻新后的设备质量和标准与新设备一致。
翻新医疗器械满足了小型医疗机构使用CT、MRI等大型设备的需求,还可以节约社会资源,利于环保及节能减排。
国外一些医械大厂商,比如GE医疗、飞利浦医疗、西门子医疗、佳能医疗,在翻新医疗设备领域,也都分别有自己一套完善的流程和机制。
GE医疗曾在其官网发文,介绍在翻新(refurbishing)、再利用(reusing)和回收(recycling)医疗设备等方面所做的工作。
当医疗机构决定拆除一台影像设备时,GE医疗可以通过其GoldSeal项目提出回购,医疗机构还能够收回一些费用。
一旦废弃设备被GE医疗购买,工程师就会拆卸掉该设备,将其运到GE医疗的一个机构,在那里将设备进行翻新(refurbished),或收集设备部件,用于维修其他在用设备。很多不可再生(reused)的材料都能被循环使用(recycled),而不必进入垃圾填埋场。
GE 医疗GoldSeal项目所翻新的设备(refurbished equipment)能够满足甚至超过原有的设备规格。与新设备相比,购买GoldSeal项目的磁共振、CT或PET/CT产品可以节省大约20%左右的采购成本。
此外,GoldSeal项目的零部件也是购买二手零部件的可靠选择,并且价格诱人。对于那些已经过时、难以找到配件的设备来说,这些二手零部件还可以延长它们的生命周期。
一台普通的“退役”CT可以拆卸出多达53个零部件。位于美国威斯康星州密尔沃基附近的GE医疗维修运营中心的团队大约需要20个小时,才能把这些零部件全部摘取出来。仅在密尔沃基的维修中心,每年就能够回收(recycled)或再利用(reusable)大约1100万磅(差不多相当于1100头大象)的“退役”医疗设备和零部件。

飞利浦Diamond Select的翻新设备包括:磁共振、CT、心脏/血管或介入X线设备、常规X线机、外科C型臂、核医学设备和PET/CT、外科移动设备(mobile surgery)、超声设备。

ecoline业务同样由五个步骤组成:选择——拆卸运输——翻新——安装——提供与新设备同样的质量保证和售后服务。
Secondlife项目在翻新过程中,先由设备所在地的授权工程师进行运行测试,出具设备状态报告,符合要求的设备才会进入Secondlife流程,由经过培训的专业人员进行拆卸,并转移到佳能医疗位于丹麦奥尔堡的翻新中心。

翻新后的设备将确保符合佳能医疗原厂的各项规格要求,最终出厂的翻新设备贴有Secondlife标识,这也是质量保证的标志,并享有一年原厂保修。

2005年《新京报》的一篇报道中曾提到,据美国Frost&Sullivan公司调查,2004年全球翻新再用医疗设备市场为12亿美元,每年以10%的速度增长硬件防火墙原理。目前该部分销售已占到全球总量的5%-7%。其中美国、欧洲两大市场各达到2.5亿美元。
到了2017年,全球翻新医疗设备市场价值为63亿美元,预计复合年增长率将超过9.7%,这一数字来自国外市场调研者Laura Weynants的数据调查。
而2018年5月由美国Prudour Pvt市场调研公司发布的报告注显示,到2020年,全球翻新医疗市场预计将达到104亿欧元。在未来5年,其年复合增长率将达到12%。在全球医疗技术市场占比约为17%。
注:报告全名为《全球翻新医疗设备市场到2026年的预测及展望——类型(手术室设备&外科设备,监护设备和除颤器)、应用(医院,诊疗中心)和地域》。
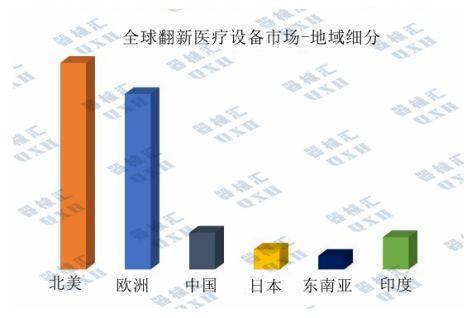
目前,翻新设备最大的消费市场来自北美,其次是德国和其他欧盟国家。不过,预计未来几年,最显著的增长将来自亚洲市场。大多数国家均在其二线城市或地区呈现出最大的增长潜力。
印度是积极接受二手和翻新产品的市场之一硬件防火墙原理,随着其医疗体系的发展,印度将继续为此类产品提供机遇。其中,澳大利亚的EverX公司和美国GE医疗在印度拥有强大的供应商网络,在印度市场占有一定优势。不过,由于印度市场的规模较大,以及其医疗市场的分散化,还远未达到饱和,其他厂商仍有充分的机会。
发展中国家的翻新医疗设备市场需求将不断增加。这是由于一些发展中国家,特别是亚太地区设备英文单词,各种医疗费用报销情况不佳造成的。
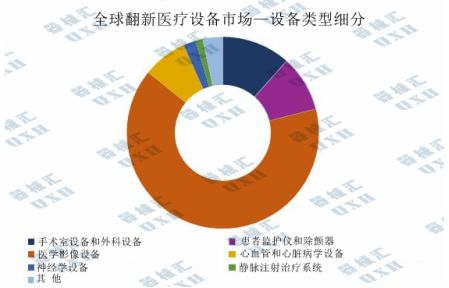
在翻新医疗设备的细分类型方面,医学影像设备占有较大份额,并将在未来几年内保持其主导地位。医学影像、心血管和神经系统等设备的成本压力较高,这是推动全球翻新医疗设备市场增长的关键因素。
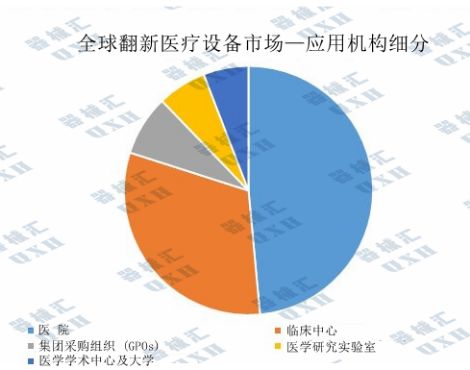
在所有应用细分市场中,医院有望成为全球翻新医疗设备市场中增长最快的细分市场。增长的主要原因是发展中国家和欠发达地区的公立、私立医院的预算限制,以及日益重视减少资本支出及购置全新医械的开销。
在中国,由于人口老龄化,以及寻求更高质量医疗服务的人数不断增加,医疗服务需求的增长将推动市场增长。此外,医疗服务也面临巨大的成本压力,医疗机构寻求更具成本效益的解决方案硬件包括哪些,这使得中国成为全球翻新医疗器械市场中的一块“肥肉”。据估计,中国翻新医疗设备市场到2020年将达到至少10亿美元的规模,200张床位以上的小型医院是翻新医疗器械最大的终端客户群体。
20世纪80年代,进口大型二手医疗设备的交易一度在我国盛行。当时的医院普遍资金匮乏,但诊断水平亟待提高,只好购买二手或翻新的CT、磁共振、X射线机等。
1996年7月23日,原卫生部(现卫健委)和国家计委(现国家发改委)联合发布了《关于加强大型医用旧设备管理有关问题的通知》,明令禁止任何形式的二手医疗设备进口和使用。
该通知要求对购置的大型医用旧设备(CT、MRI、X刀、γ刀),必须取得《大型医用设备配置许可证》、《大型医用设备上岗人员技术合格证》和《大型医用设备应用质量合格证》(简称“三证”)后方可使用,1996年12月31日前未取得“三证”的大型医用设备,要停止使用。
此外,2001年12月27日,原外经贸部、海关总署、原国家质检总局发布《禁止进口货物目录》(第二批)旧机电产品禁止进口目录,禁止包括医疗设备在内的二手机电产品进口设备英文单词。
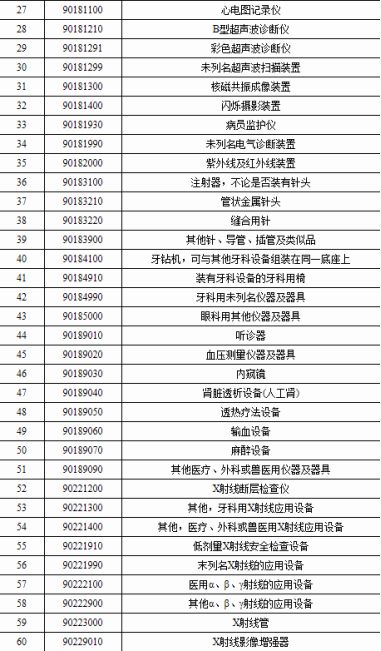
这些措施在当时极大遏制了二手医疗设备市场的发展,客观上扶持了本土企业在中低端CT、磁共振、监护仪、超声仪等影像设备领域的崛起。
2005年4月,当时的国家食品药品监管局出台了《翻新再用医疗器械监督管理规定(征求意见稿)》(以下简称“《规定》”),其中,对翻新再用医疗器械的定义是:已使用过,由原生产企业或其委托的企业收回、翻新后再次销售、使用的医疗器械。

2005年4月26日,来自全国各地的药监局和医疗器械检测中心代表、跨国公司、本土厂商近80人参加了由国家药监局主办的“翻新再用医疗器械监管研讨会”。
当时的北京万东、北京医疗器械研究所、深圳迈瑞生物、深圳安科等国内公司的6名代表,以及GE、西门子、飞利浦、贝克曼库尔特等国外巨头的高管均参加了会议。
6月19日,中国医疗器械协会联合深圳市医疗器械行业协会,共计41个单位60余名代表,在深圳召开第二次研讨会,并在会后形成一份《关于规定情况的紧急报告》。
6月22日,国家药监局召开局机关正处级以上干部、直属单位主要负责人的大会,中组部一位副部长到会宣布,免去的SFDA党组、局长职务,其职务由邵明立接任。
6月27日,在中国医疗器械行业协会的推动下,本土厂商获得与SFDA医疗器械司官员直接对话的机会。不过,此次会议一度进入僵持状态。一位与会者回忆,时任国家食品药品监督管理局医疗器械司司长的郝和平推行《规定》的态度相当强硬:“你们可以怀疑我的执政能力,但不该怀疑我的执政立场。”
在磋商未果的情况下,6月27日同一天,国内众厂商商务部,明确反对《规定》出台,送达资料多达20多套,联名企业包括当时的东软数字医疗、上海医疗器械厂、北京万东医疗等数十家。
作为《规定》的主要起草者和力荐者,郝和平的意外落马硬件包括哪些,使得曾经被业内人士预测将于当年7月末正式出台的《规定》也因此而搁置不谈。
2008年4月20日,“中国再造医疗设备之未来”小型圆桌闭门会议在深圳召开,以中国欧盟商会、COCIR牵头的多家知名跨国医疗设备生产商代表,和由国内行业协会领衔的中国本土高值医疗器械企业代表、部分医院的代表以及中国医学装备协会和中国医药卫生事业发展基金会的代表共20多人,就中国医疗设备的翻新再造展开激烈争辩。
此次圆桌会从节约资源的角度肯定了医疗设备的回收再利用,但在翻新再造方面,由于各方分歧较大,未达成一致意见。
2000年1月4日,被称为“医疗器械行业母法”的《医疗器械监督管理条例》,经1999年12月28日国务院第24次常务会议通过,予以发布,自当年4月1日起施行。
其中第二十六条规定,医疗器械经营企业不得经营未经注册、无合格证明、过期、失效或者淘汰的医疗器械。医疗机构不得使用未经注册、无合格证明、过期、失效或者淘汰的医疗器械。

由于大部分大型医疗设备没有有效期的规定,检验检测较难操作,对于淘汰医疗设备也未公布过目录。因此,对“过期、失效、淘汰以及检验不合格”这些情形都难以作出区分界定,导致这一规定在施行过程中难免流于形式。
2014年3月7日,《医疗器械监督管理条例》在十四年后予以修订,经国务院第39次常务会议修订通过,正式发布,自当年6月1日起执行。

2014版《医疗器械监督管理条例》的第四十一条规定:医疗机构使用单位之间转让在用医疗器械,转让方应当确保所转让医疗器械安全、有效,不得转让过期、失效、淘汰以及检验不合格的医疗器械。

这条规定,业界普遍认为是给予了争议颇多的“二手医疗器械”一个合法名分,是对二手医疗器械使用的“有限认可”。
与2000年版《医疗器械监督管理条例》相比,2014版《条例》对“过期、失效、淘汰以及检验不合格的医疗器械”仍未做出明确定义。
从实际情况来看,真正属于医疗机构之间转让医疗器械的行为并不多,大部分交易行为都是一些中介公司在操作。这些通过中间商转让、销售的二手医疗器械很难确保其质量安全。
2017年5月19日,中央政府网发布了由李克强总理签署的《中华人民共和国国务院令第680号》,即《国务院关于修改医疗器械监督管理条例的决定》。


2017年10月31日,食品药品监管总局办公厅发布《〈医疗器械监督管理条例〉修正案(草案征求意见稿)》(以下简称“《草案征求意见稿》”),公开征求意见。

(1)将第四十一条改为第四十五条,并增加一款作为第一款:“医疗器械使用单位不得使用未依法注册、无合格证明文件以及过期、失效、淘汰的医疗器械。”
(2)加强旧医疗器械监管。进一步加强对旧医疗器械的监管,明确禁止经营已使用的医疗器械(第四十四条、第七十一条)设备英文单词。
《草案征求意见稿》进一步加强了对二手医疗器械的监管,明确禁止经营已使用的医疗器械,并明确了处罚标准(第七十一条)。
一旦经营无合格证明文件、已使用的医疗器械(即包含翻新和二手医械),将面临重罚。如前文所述,MRI和CT是最常见的翻新医械,价格本身就不菲,而罚金将至少在其货值金额的5倍以上,最多可高达10倍。
2018年6月25日-7月24日,市场监管总局报请国务院审议的《医疗器械监督管理条例修正案(草案送审稿)》(以下简称“《草案送审稿》”)公开征求意见。
其中,《草案送审稿》将第四十二条改为第四十八条,增加两款,作为第三款和第四款:“医疗机构临床急需,需要进口医疗器械,按照国家有关规定办理进口手续。”“禁止进口和销售已使用过的医疗器械。”
此前,由于法律法规未明确禁止进口和销售已使用的医疗器械,2001年颁布的《禁止进口货物目录》(第二批)中,旧机电产品目录又不能涵盖大部分医疗器械,存在对非法进口旧医疗器械面临定性难、处理难的突出问题设备英文单词。这次的《草案送审稿》对这个问题做出了明确规定。
进口的医疗器械应当有中文说明书、中文标签。说明书、标签应当符合本条例规定以及相关强制性标准的要求,并在说明书中载明医疗器械的原产地以及代理人的名称、地址、联系方式。没有中文说明书、中文标签或者说明书、标签不符合本条规定的,不得进口。
这里多提一句,2018年12月26日,商务部、海关总署对禁止进口的旧机电产品目录进行了调整,发布了新的《禁止进口的旧机电产品目录》(2019年1月1日起执行),上文提到的2001年外经贸部、海关总署、质检总局公布的《禁止进口货物目录(第二批)》同时废止。


此外,近年来,借老龄化社会的康复护理需求爆发,康复辅助用途的医疗器械租赁市场也在蓬勃发展。一些医疗器械经营连锁企业,既有医疗器械的传统销售,也在拓展康复辅助用医疗器械的租赁、回收、经营业务。《草案送审稿》中第八十六条规定:“康复辅助器具类医疗器械的范围及其管理办法,由国务院食品药品监督管理部门会同国务院民政部门依据本条例的规定制定。”
2014年4月,当时的国家食品药品监管总局召开医疗器械“五整治”专项行动第二次新闻发布会,通报对部分医疗器械经营企业和使用环节的暗访调查和查处情况,以及专项行动中查处的五个典型案件情况。
其中包括非法经营商在香港注册公司,从国外进口一些淘汰的二手彩超机,然后经过维修硬件包括哪些、改装和翻新以后,又贴上通用、富士等品牌的商标,冒充国内某合法的经营企业资质来销售。这类情况的目标往往指向中小型医疗机构,主要是乡镇卫生院、私人诊所。
时任国家食品药品监督管理总局稽查局局长的毛振宾当时曾表示,只要在网上监测到(医疗器械违法案件),发现一起查一起,绝不会手软,决不会姑息。
河南省新乡市食药监局联合新乡市公安局,成功侦破一起非法经营和销售伪劣三类医疗器械案,收缴美国通用彩超机、B超机、日本富士CR等二手医疗器械洋垃圾48台,涉案价值近1500万元。
上海食药监局浦东新区分局联合门破获了林某等非法经营翻新CT机等医疗器械案,查获已翻新及准备翻新的GE、西门子等品牌CT机23台,洗片机22台和超声诊断仪5台,物品货值人民币625万余元。
11月10日,海关总署缉私局统一指挥北京等11省市的海关缉私局,共同开展打击走私翻新医疗设备的专项活动,抓获犯罪嫌疑人32名,起获翻新医疗设备400余套,案值约3.8亿元人民币。
12月16日,北京市检察院第四分院对5件涉嫌走私翻新医疗器械案的嫌疑人高某等7人,以走私国家禁止进出口的货物罪作出批准逮捕决定。这5起案件是上述案件中的一部分,涉案走私翻新医疗设备,主要包括彩色诊断仪、机百余台,涉案金额8000余万元。
云南省药监局经过逐一摸排,锁定23台某国际大品牌的进口彩色超声诊断仪涉嫌为走私翻新旧医疗设备,其中8台货值金额700多万元的走私翻新的医疗设备已交辖区药监部门查处。
山东省潍坊市2家医疗机构涉嫌使用无证医疗器械而被处罚硬件防火墙原理。1家是乡镇卫生院,1家是县级人民医院,所使用的彩色超声诊断仪(型号:LOGIQ P6)均被查出为未经注册的医疗器械。
湖北省某医院所使用的标识为GE品牌、型号LOGIQ P5 和Vivid E9 的彩超,被查出为经过翻新的医疗设备,中文铭牌上的产品注册号无效硬件防火墙原理。
贵州省某医院因为购买、使用未依法注册的“超声诊断仪”被开罚单。该院以72万元购进的标识为GE品牌的Voluson E6彩超,经查是将已使用多年的旧设备进行了翻新,产品序列号不存在,中文铭牌属于伪造。最终该台彩超被没收。
拉萨海关与自治区、林芝市食品药品监督管理部门及拉萨市、林芝市卫生行政主管部门开展联合执法行动,分别在拉萨、林芝两地医院查获了临床使用的,涉嫌走私进境的翻新四维彩超机2台、手术机1台,案值共计人民币200余万元。拉萨海关缉私部门对涉嫌走私翻新医疗设备进境的2家进口企业依法开展刑事立案侦查。
二手医疗器械:目前我国法律法规对二手医疗器械没有确切定义,一般指医疗机构更新替换下来的大型医用设备。上文《医疗器械监督管理条例》中的相关条款用词为“已使用过的医疗器械”。
在我国,二手医疗器械往往以转让、合作、租赁、捐赠等方式流向落后地区的县乡综合医院和民营医院。购买二手医疗器械虽然价格便宜,但是其安全性和有效性难以保证。
翻新医疗器械:在最终未能落地的《翻新再用医疗器械监督管理规定(征求意见稿)》中,对翻新医疗器械的定义为:“已使用过,由原生产企业或其委托的企业收回、翻新后再次销售、使用的医疗器械。”
翻新医械与二手医械有着本质的区别。翻新医械需要经过严格的工作流程,并通过性能测试,达到注册标准后才能出厂,并享有售后服务。翻新再造的医疗设备与新生产的设备一样,需要通过监管部门的注册登记和质量监管。
单纯的二手医疗器械无法保证其安全性和有效性,但翻新医疗器械则不同,从循环经济的角度看,医疗器械的翻新再利用存在现实、正向的一面。然而,对于大多数中国医疗器械生产企业来说,这可能还是一个无暇顾及的领域。我国医疗器械行业处于创新发展的关键时期,大部分中国企业的产品面向中低端市场。翻新医械价格比同等全新医械低20%左右,是中低端市场的最有力竞争者。我国对翻新医械市场的延迟开放,为民族医疗器械企业赢得了宝贵的发展时间。
免责声明:本站所有信息均搜集自互联网,并不代表本站观点,本站不对其真实合法性负责。如有信息侵犯了您的权益,请告知,本站将立刻处理。联系QQ:1640731186



